

Modelo teórico de respuesta inmunológica en la mucosa
gastrointestinal en la infección por H. pylori
El mecanismo patogénico responsable de la amplia diversidad de manifestaciones clínicas de H. pylori aún no está totalmente esclarecido, así como tampoco ha logrado establecerse un modelo teórico que justifique la respuesta inmunológica que tiene lugar en la mucosa gástrica, una vez que es invadida por esta bacteria. Por ello se propone el siguiente modelo teórico en el que suponemos que la cepa causante de la infección sea CagA positiva (CagA+) la cual tiene una mayor capacidad de inducir una respuesta inflamatoria e inmune en la mucosa gástrica, pero igualmente se han asociado a una mejor respuesta a la terapéutica de erradicación, ya que las VacA positivas (VacA+) se caracterizan por ser menos citotóxicas o patogénicas.
Una vez dentro de la interfase mucosa gastrointestinal, H. pylori es capaz de mediar procesos de adhesión, colonización y multiplicación. Estos procesos generalmente cursan con una clínica caracterizada por: gastritis, úlceras pépticas y en casos más severos puede llegar hasta adenocarcinoma gástrico. La colonización inicial se ve facilitada por el bloqueo de la producción de ácido por una proteína bacteriana inhibidora de ácido (ureasa) la cual protege a la bacteria de los efectos letales del ácido gástrico mediante la formación de una nube de amonio que le sirve para tamponar su entorno vital y colonizar el epitelio. La actividad ureasa está aumentada por una proteína del shock por calor (HspB, por sus siglas en idioma inglés) que se expresa conjuntamente con ésta en la superficie de la bacteria. El daño tisular localizado está mediado por los residuos de ureasa, mucinasa, fosfolipasas, además de las proteínas VacA y CagA, que inducen el daño de las células epiteliales y que, conjuntamente con la ureasa y el lipopolisacárido bacteriano, estimulan una respuesta de tipo inflamatoria (3).
La
patogénesis de dicha respuesta inflamatoria incluye 2 fases:
Una primera fase está
caracterizada por la llegada y penetración del microorganismo al
mucus gástrico donde se asienta y multiplica. En esta etapa, H.
pylori libera varias sustancias tóxicas que son capaces de
estimular una respuesta inmunológica local, expresada en un aumento
de IgA secretora (principal inmunoglobulina de las mucosas), con el fin
de evitar el proceso infeccioso. Las principales células inflamatorias
participantes en este proceso inicial son los neutrófilos, que
son atraídos al sitio de la lesión; de ahí que su
presencia en compañía de folículos linfoides se considere
como “signo de actividad”. Durante esta fase es frecuente
observar la invasión de H. pylori en las células
epiteliales.
Hay una segunda fase caracterizada por una amplificación de la respuesta inflamatoria, debido a la interacción de linfocitos, neutrófilos, macrófagos y células mastoides que, al ser atraídos al sitio de la lesión, liberan gran variedad de mediadores químicos como: citocinas, eicosanoides, metabolitos reactivos de oxígeno (radicales libres del oxígeno) y activación del sistema o cascada de complemento (C') que perpetúa la inflamación. En esta última etapa, también participan los neuropéptidos liberados por las neuronas del sistema nervioso entérico, que contribuyen a ampliar la respuesta inflamatoria y aumentan los daños funcionales del estómago colonizado por H. pylori.
Esta última etapa es importante en la patogénesis de la inflamación gástrica y resalta la participación del sistema inmune local y sistémico en el control de la infección y la neutralización de las toxinas bacterianas. Además, se potencia la destrucción hística que según su intensidad y duración, puede crear una úlcera gástrica (15).
Por otro lado, en la búsqueda de patrones de respuesta del huésped frente a una infección por H. pylori, se ha encontrado que existe una amplia gama de factores que juegan un rol fundamental en la defensa del organismo frente a la bacteria, los cuales pueden generar distintas respuestas. De ellos, la IL-8, una quimiocina perteneciente a la familia C-X-C, actúa como quimioatrayente en la inmunopatogénesis de la gastritis induciendo la migración de polimorfonucleares (PMN) frente a una infección por H. pylori. También la producción de IL-8 está relacionada con la permeabilidad celular, puede reclutar y activar neutrófilos y aumentar la interacción de la bacteria con células de la lámina propia, incluyendo macrófagos y células pertenecientes al linaje linfoide. De la misma manera, citocinas como IL-6 han estado asociadas con un incremento de su producción frente a la bacteria induciendo una inflamación crónica, con una severa infiltración de PMN y células mononucleares (MNC). Efectos sistémicos también se han relacionado a la producción de mediadores inflamatorios como lo es el factor de necrosis tumoral alfa (TNFα).
De igual forma, H. pylori es capaz de activar y promover la diferenciación de linfocitos Th0 (CD4+) los cuales, según el patrón de citocinas presentes en el medio y de las condiciones inmunológicas propias del individuo, pueden diferenciarse en Th1 mediando una respuesta de tipo celular o bien Th2 con una respuesta de tipo humoral. La respuesta celular es mediada a través de citocinas tipo Th1 -tales como IFNγ, IL-2 y TNFα-, mientras que las citocinas tipo Th2 -como IL-4 e IL-5- promueven una respuesta de tipo humoral. Pero el potencial o tipo de respuesta inducida por H. pylori aún no está totalmente esclarecido, razón por la cual probablemente la respuesta inmune ocasionada por la invasión de este microorganismo a la mucosa gastrointestinal suponga un equilibrio entre la línea celular y humoral, sin dejar de vista la típica respuesta inflamatoria que es característica de tal infección. Esto es debido a que en algunos pacientes suele encontrarse una respuesta inflamatoria persistente sin daños mayores, mientras que en otros puede haber una respuesta humoral o celular, teniendo ésta última importantes implicaciones en el desarrollo del cáncer gástrico.
A
nivel de la respuesta celular, se proponen dos mecanismos:
1.-
La fagocitosis para presentación
antigénica, la cual es llevada a cabo por macrófagos, grupo
celular que actúa como células presentadoras de antígenos
(CPA) cuya función es presentar los antígenos de H.
pylori a los linfocitos T circulantes. Pero como los macrófagos
no resisten el ácido gástrico y los determinantes de virulencia
o patogenicidad de la bacteria son muy potentes, la fagocitosis se ve
frustrada. Por esto no se considera un mecanismo con una fase efectora
lo suficientemente “efectiva” como para eliminar a la bacteria,
ya que todo el proceso de respuesta inmunológica desencadenado
queda en la presentación antigénica y cuando hay producción
de anticuerpos con previa estimulación de células o linfocitos
B, estos anticuerpos no resultan lo suficientemente efectivos como para
contrarrestar el proceso infeccioso ocasionado por tal invasión,
ya que los mismos son incapaces de atravesar la mucosa gástrica
y remediar de esta forma el daño producido.
2.-
La apoptosis o muerte celular
programada con el fin de mantener estable el número de células
gástricas epiteliales y así una proliferación celular
balanceada. Este mecanismo es de tipo citotóxico, es decir, media
citotoxicidad a través de los linfocitos CD8+, los cuales expresan
en su superficie FasL, mientras que las células epiteliales infectadas
expresan Fas.
En este mecanismo, el Fas expresado por la célula epitelial interactúa
con el FasL del linfocito T CD8+ y produce una cascada de eventos que
resultan con la apoptosis celular. Este proceso apoptótico está
asociado a la activación de las caspasas, específicamente
la caspasa-3 que es conocida como una pieza clave dentro de la cascada
apoptótica, ya que esta proteína activa DNAsas citoplasmáticas,
las cuales subsecuentemente migran al núcleo y degradan el ADN.
Se ha propuesto un mecanismo que sugiere que el aumento de TNFα debido
a la infección de la mucosa gástrica por H. pylori,
contribuiría al aumento de la apoptosis celular y la actividad
de la caspasa-3, vía la activación de la caspasa-8. De igual
manera la activación de células T, especialmente de tipo
Th1, por esta infección que expresan FasL y el sistema Fas-FasL
aumentarían la apoptosis (16).
Dicho mecanismo apoptótico supone una importante línea de defensa para evitar la proliferación de células epiteliales gástricas malignas que dan lugar a procesos neoplásicos, es decir, cáncer. De igual forma, se han hecho diversos estudios y propuesto diversos postulados sobre el posible efecto de la toxina de vacuolización VacA (que media la vacuolización de las células epiteliales gástricas) que, dependiendo de su concentración en el medio, es capaz de mediar el fenómeno apoptótico de tales células, fenómeno que queda o está por ser demostrado en estudios sucesivos.
Tal propuesta está basada principalmente en la existencia de 2 factores condicionantes, como los son: la duración del proceso infeccioso (tiempo-dependiente) y la concentración de la toxina, donde una asociación de largo tiempo con el proceso infeccioso con una alta expresión y concentración de tal toxina aumentarían el proceso apoptótico, y por el contrario se vería disminuido si tales factores condicionantes también se presentan en menor grado o proporción (17).
El programa de muerte celular está regulado por señales desde otras células, las cuales pueden activarlo o suprimirlo. Estas interacciones célula-célula son parte del complejo control “social” que garantiza que las células individuales trabajen para el bien del organismo como un todo. En el estudio de los mediadores moleculares de la apoptosis se ha visto un aumento de la expresión del supresor tumoral p53 y de la proteína pro-apoptótica Bak en respuesta a la infección por H. pylori.
La proteína p53 es esencial para la inducción de apoptosis como respuesta a un daño cromosómico. Actúa por bloqueo de la replicación del ADN de las células dañadas. Si las lesiones del cromosoma no pueden ser reparadas en cierto tiempo, las células mueren por apoptosis. El gen que codifica el p53 está inactivado por mutación en el 50% de los cánceres humanos incluyendo los gástricos, lo que permite a las células cancerosas sobrevivir y proliferar aún cuando su ADN esté dañado; lo que favorece la acumulación de futuras mutaciones. La diferencia en la expresión de p53 tiene similares efectos a la sobre expresión del Bcl-2. Los altos niveles de Bcl-2 promueven cáncer por inhibición de apoptosis, prolongando, de este modo, la supervivencia celular. Ahora está bien establecido que el Bcl-2 es el miembro prototipo de una gran familia de genes que codifican proteínas que pueden inhibir (p.e Bcl-2, Bcl-xl) o promover (p.e Bax, Bcl-xs, Vak) la apoptosis. La sobre expresión de Bcl-2 puede conducir a células resistentes a la apoptosis y de ese modo favorecer el crecimiento maligno. Hay recientes publicaciones que relacionan esta familia de proteínas con la regulación del proceso de apoptosis inducido por H. pylori (18).
Por otro lado, la estimulación de células Th0 por citocinas como IL-4 e IL-5 trae como consecuencia que se lleve a cabo su proceso de diferenciación en células plasmáticas productoras de anticuerpos. Esto desencadena una respuesta de tipo humoral caracterizada por la producción de anticuerpos bien sea específicos para toda la bacteria (típicos de especie) o para un determinante de patogenicidad en particular; ya que se ha demostrado que existen patrones de IgG para H. pylori, así como también IgG específica para CagA por ejemplo.
De igual forma, cabe recalcar que durante la infección por H. pylori pueden producirse inmunoglobulinas de diversos tipos que median diferentes procesos o activan diversos mecanismos efectores. Así, por ejemplo, la IgA juega un importante papel en la facilitación de la fagocitosis, además de su importancia como principal inmunoglobulina de las mucosas y actúa como una primera línea de defensa ante diversos agentes patógenos (es de suma utilidad en el diagnóstico no invasor de la infección a partir de muestras de saliva en niños). La IgE media hipersensibilidad tipo I (reacciones alérgicas), ya que H. pylori está asociado al desarrollo de la urticaria y otras enfermedades extragástricas que cursan generalmente con procesos alérgicos, además de su papel como inmunoglobulina en la citotoxicidad mediada por anticuerpos (ADCC); sin embargo no parece ser una de las inmunoglobulinas importantes en la génesis de las enfermedades extragástricas asociadas a la bacteria (p. ej. urticaria crónica idiopática), pues los niveles de IgE específica anti-H. pylori no se asocian proporcionalmente a severidad de la patología o respuesta a la erradicación del microorganismo (19). La IgG por su parte activa la vía clásica del complemento (C'), lo que favorece la opsonización y por ende el proceso de fagocitosis (es la principal inmunoglobulina empleada en diagnóstico y seguimiento). Y, finalmente, la IgM está presente en los pacientes que cursan por primera vez con la infección causada por H. pylori (esta positividad es inusual en nuestro país debido a lo temprano de la primoinfección y a la falta de pesquisa de la misma).
Presentamos, en la figura 2, un resumen del modelo teórico de las vías propuestas para el desarrollo de la respuesta inmunológica en la infección gástrica por H. pylori.
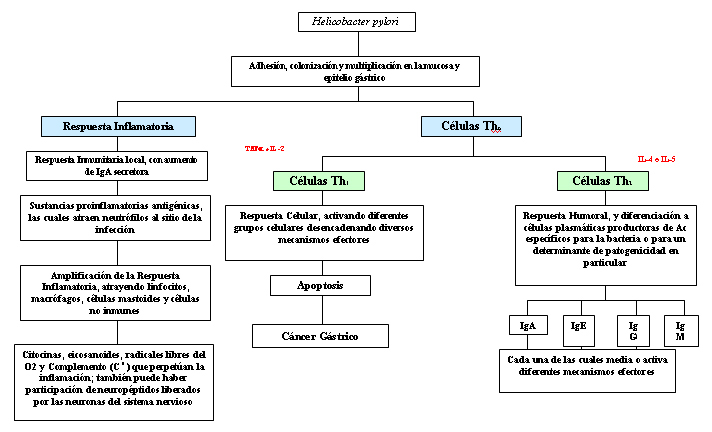
Figura
2 |
