

![]()
Alteraciones
Neuroendocrinas y del Sistema Inmune
Las Alteraciones Neuroendocrinas Contribuyen a la Génesis Biológica de la Enfermedad Depresiva.
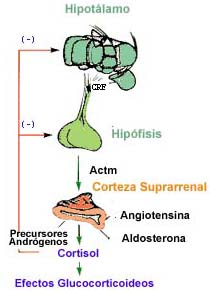
La depresión se asocia con signos de alteración hipotalámica (20) que se manifiesta en una secreción excesiva de corticotropina (ACTH) por la hipófisis, induciendo aumento de la secreción de cortisol por la corteza suprarrenal. La secreción de ACTH es tan importante que en algunos pacientes deprimidos se puede observar aumento del tamaño de la glándula suprarrenal por medio de tomografía axial computarizada (TAC) (21).
La secreción normal de cortisol sigue un ritmo circadiano, alcanzando un pico máximo a las 8:00 AM, siendo menor en la tarde y en la madrugada. Este ritmo se encuentra alterado en el 50% de pacientes deprimidos, los cuales excretan grandes cantidades de cortisol a lo largo de todo el día (21), incluso mientras duermen. La administración oral de dexametasona no ocasiona en los pacientes deprimidos la supresión normal de la producción de cortisol. Cerca de 40-50% de los pacientes continúan con niveles altos de cortisol después de recibir 1, 2 u 8 mgs de este esteroide sintético.
El aumento de la secreción de cortisol es el resultado final de la hipersecreción de la hormona liberadora de corticotropina (CRH) en el hipotálamo. Recordemos que la CRH aumenta los niveles de ACTH, con las consecuencias ya mencionadas. Los niveles de CRH se correlacionan con la depresión, pues la liberación de esta hormona es estimulada por la noradrenalina y la acetilcolina. Por esta razón, se infiere que la CRH y el sistema noradrenérgico se refuerzan entre sí (22).
Las Alteraciones del Sistema Inmune se Suman a las Modificaciones Neuroendocrinas
de la Depresión.
Se ha demostrado una alteración del eje Hipotálamo-Hipófisis- Suprarrenal (HHS) mediada por citoquinas, que son mensajeros químicos diversos y potentes secretados por las células del sistema inmunológico, entre los cuales se encuentran los linfocitos, las células T, las células B, los monocitos y los macrófagos.
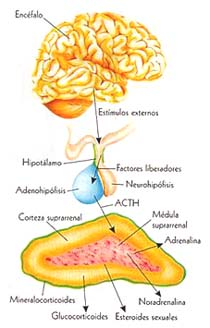 Estas
pueden activar el eje HHS, directa o indirectamente. Directamente, a través
de sus efectos sobre el CRH (24); indirectamente, por medio de la resistencia
de los receptores a los glucocorticoides, inducida por citoquinas (25,26), originando
hiperactividad del eje HHS y afectando así su inhibición por retroalimentación
(27, 28).
Estas
pueden activar el eje HHS, directa o indirectamente. Directamente, a través
de sus efectos sobre el CRH (24); indirectamente, por medio de la resistencia
de los receptores a los glucocorticoides, inducida por citoquinas (25,26), originando
hiperactividad del eje HHS y afectando así su inhibición por retroalimentación
(27, 28).
Las citoquinas proinflamatorias, como la IL-6, pueden alterar los neurotransmisores en múltiples regiones del cerebro (29), debido a que esta última contribuye a reducir la disponibilidad de L-triptófano (30), disminuyendo así la disponibilidad de serotonina en el SNC.
Por otro lado, los receptores de citoquinas se expresan en neuronas del SNC, lo que genera la posibilidad de que las citoquinas funcionen como neurotransmisores (30) y ejerzan efectos directos sobre el SNC.
También se ha pretendido darle una localización neuroanatómica a la depresión. Así, los estudios de tomografía por emisión de positrones (PET) y de resonancia magnética funcional (RMf) han determinado una posible alteración anatómica en la corteza prefrontal ventral a la rodilla del cuerpo calloso, alterada en los casos de depresión unipolar. Durante la fase depresiva de la enfermedad, la actividad en esta región disminuye. Esta disminución parece explicarse en gran parte por la reducción del volumen (45% aprox.) de la sustancia gris de esta zona de la corteza prefrontal (31).
Esta región de la corteza prefrontal tiene extensas conexiones con otras regiones involucradas en la conducta emocional, como el núcleo amigdalino, el hipotálamo lateral, el núcleo accumbens y los sistemas noradrenérgicos, serotoninérgicos y dopaminérgicos del tronco encefálico. Las personas con lesiones en estás áreas presentan dificultades para experimentar las emociones (31).
Dentro de los factores biológicos señalados anteriormente, es importante detenerse en el sistema inmunológico, recordar algunos conceptos básicos y entender sus alteraciones presentes en el trastorno depresivo mayor. Además, se revisará la importancia de la serotonina en la fisiopatología de la depresión y su relación con el sistema inmune.
Se conoce con el término inmunidad al estado fisiológico de reacción y reconocimiento de toda sustancia extraña por parte de un ser vivo. Tales elementos exógenos o foráneos son denominados antígenos. Se consideran antígenos a una amplia variedad de elementos, entre los cuales pueden incluirse microorganismos patógenos o macromoléculas de naturaleza proteíca o polisacárida, no necesariamente asociados con el desarrollo de enfermedades (38).
El reconocimiento de todo antígeno, definido de manera genérica como respuesta inmunitaria, se lleva a cabo a través de diferentes eventos celulares y moleculares. Las células y moléculas responsables de tal respuesta constituyen el sistema inmune (38).
El efecto de reconocimiento y protección contra un antígeno determinado se lleva a cabo a través de dos tipos de respuesta inmunitaria: respuesta inmune innata y respuesta inmune adaptativa (38).
La repuesta inmune innata o natural se desarrolla como primera línea de defensa contra antígenos con actividad patógena. Se caracteriza por un efecto inmediato, cuya actividad no es estimulada exclusivamente por exposición al antígeno, ya que sus elementos efectores constitutivos existen en el organismo antes de producirse el desafío antigénico (38).
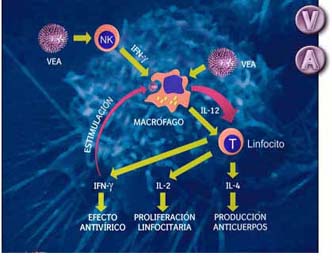
Entre los factores efectores de la respuesta se encuentran: 1) Barreras fisicoquímicas, como la piel y mucosas. 2) Moléculas circulantes, como el complemento. 3) Células, como fagocitos mononucleares (macrófagos), polimorfonucleares (neutrófilos) o células asesinas naturales (Células NK o “natural killer cells”). 4) Factores humorales, como gamma-Interferon o Factor de Necrosis Tumoral (“Tumor Necrosis Factor” o TNF) (38).
La respuesta adaptativa o específica se caracteriza por la capacidad de reconocer antígenos con alta especificidad y desarrollar memoria inmunológica. Dicha respuesta se activa e incrementa de manera determinante ante la exposición al antígeno. Entre los principales componentes de la respuesta adaptativa se encuentran: 1) Células de la serie linfocitaria (Linfocitos T o B) y 2) Factores humorales como los anticuerpos (38).
La respuesta específica se clasifica a su vez en dos tipos: 1)Respuesta inmune celular específica, mediada por Linfocitos T y 2) Respuesta humoral o B-dependiente. Para iniciar una respuesta específica, tanto los linfocitos B como los T deben llevar a cabo procesos de activación, diferenciación y proliferación, con el estímulo del antígeno, ya sea por efecto de factores solubles conocidos como interleuquinas o a través de fenómenos de interacción por contacto específico con determinantes de superficie expresados por otras células “nodrizas” o inductoras (38).
 La
inmunidad celular contra un antígeno puede ser transferida a individuos
“vírgenes” (es decir, que no han sido previamente expuestos
a tales moléculas) si éstos son inoculados con células
de sangre completa o linfocitos T de un donante inmunizado con el antígeno,
pero no a través del plasma o suero del mismo. Por el contrario, la inmunidad
humoral sólo se adquiere cuando se transfiere suero o plasma de un donante
inmunizado a un individuo virgen, pero no a través de células
sanguíneas (38).
La
inmunidad celular contra un antígeno puede ser transferida a individuos
“vírgenes” (es decir, que no han sido previamente expuestos
a tales moléculas) si éstos son inoculados con células
de sangre completa o linfocitos T de un donante inmunizado con el antígeno,
pero no a través del plasma o suero del mismo. Por el contrario, la inmunidad
humoral sólo se adquiere cuando se transfiere suero o plasma de un donante
inmunizado a un individuo virgen, pero no a través de células
sanguíneas (38).
Los linfocitos T son los principales componentes de la respuesta celular específica. Son conocidos también como células T o timo-dependientes ya que su diferenciación y selección se lleva a cabo a nivel del timo. Células madre pluripotenciales, provenientes de la médula ósea, ingresan al timo para iniciar la diferenciación celular de los Linfocitos T. En el interior de la corteza, los timocitos existen en forma de una línea celular única que contiene los marcadores T: CD11, CD10, CD8, CD6, CD4 y CD5 (39). La maduración definitiva de las células T acontece primordialmente a nivel de órganos linfoides secundarios como ganglios linfáticos y bazo (38). Posteriormente, las células T en sangre periférica pueden ser clasificadas en dos poblaciones: CD4+ y CD8+. Las primeras representan el 65% de las células T; las segundas, representan el 35% restante (43). Los linfocitos T reconocen predominantemente antígenos peptídicos que han sido previamente procesados y seleccionados por células presentadoras de antígenos (CPA), tales como células de Langerhans y macrófagos (38). Más adelante volveremos a abordar los linfocitos T CD4 + y CD8+.
Las células B o bursa-dependientes, componente primordial de la respuesta inmune humoral, son las responsables de la producción de anticuerpos. Estas últimas corresponden a moléculas glicoprotéicas circulantes en sangre periférica, que reconocen predominantemente antígenos solubles. El desarrollo ontogénico de las células B se lleva a cabo a nivel de médula ósea, mientras que los eventos finales de maduración ocurren en órganos linfoides secundarios (38).
Por otra parte, la respuesta inmune celular específica se verá afectada por la serotonina, ya que los Linfocitos T poseen receptores y transportadores para este neurotransmisor, que a su vez esta relacionado con los trastornos psiquiátricos, particularmente con la depresión.
En cuanto a los receptores de serotonina, es preciso mencionar que se han encontrado 7 subtipos de receptores (5-HT1, 5-HT2, 5-HT3, 5-HT4, 5-HT5, 5-HT6 y 5-HT7). Los del tipo 5-HT1 se clasifican en 5-HT1A, 5-HT1B, 5-HT1C, 5-HT1D, 5-HT1E, 5-HT1F. Los receptores 5-HT2 se dividen en 5-HT2A, 5-HT2B, 5-HT2C (34).
Los del tipo 5HT1 han sido implicados en los procesos de relajación y contracción muscular (34). El subtipo 5HT1A particularmente interviene en la regulación de funciones cerebrales como la conducta sexual, desarrollo de episodios depresivos, estados de agresión e hipotensión ortostática, entre otros (45). Dicho receptor se ha caracterizado por el uso de ligandos marcados con isótopos radiactivos, como la [3H]-buspirona, [3H]-espiperona, a través de ensayos de afinidad (19).
La serotonina actúa sobre receptores pre y post sinápticos una vez que se encuentra en la hendidura sináptica, siendo retirada de este espacio por medio de su recaptación, evitando de esta forma que continúe la neurotransmisión (34).
 Como
se mencionó anteriormente, se ha descrito la presencia de receptores
5HT1A y 5HT2 en linfocitos T (46, 47). Los receptores 5HT1A regulan la actividad
de la adenil ciclasa. La activación in vitro de la serotonina disminuye
la actividad de la adenilato ciclasa y, por lo tanto, reduce los niveles intracelulares
de AMP cíclico (cAMP) (24). El CAMP es un segundo mensajero intracelular
con varias funciones en la célula (48). En las células T, la síntesis
de CAMP produce la activación de la protein kinasa a (pka), de la protein
kinasa c y la inactivación del metabolismo del fosfato de inositol (49),
lo cual ha sido asociado con la inhibición de la proliferación
celular e inducción de fenómenos de citotoxicidad (49).
Como
se mencionó anteriormente, se ha descrito la presencia de receptores
5HT1A y 5HT2 en linfocitos T (46, 47). Los receptores 5HT1A regulan la actividad
de la adenil ciclasa. La activación in vitro de la serotonina disminuye
la actividad de la adenilato ciclasa y, por lo tanto, reduce los niveles intracelulares
de AMP cíclico (cAMP) (24). El CAMP es un segundo mensajero intracelular
con varias funciones en la célula (48). En las células T, la síntesis
de CAMP produce la activación de la protein kinasa a (pka), de la protein
kinasa c y la inactivación del metabolismo del fosfato de inositol (49),
lo cual ha sido asociado con la inhibición de la proliferación
celular e inducción de fenómenos de citotoxicidad (49).
Se ha demostrado que la serotonina induce la secreción de Interleukina 16 (IL -16) en los linfocitos humanos T CD8+, mas no en los T CD4+ (50).
En relación al transportador de serotonina, éste tiene la propiedad de realizar un transporte activo secundario dependiente de sodio y de alta afinidad, muy sensible a la inhibición de un grupo selectivo de antidepresivos (ISRS) (47). Estos transportadores se encuentran en las neuronas del sistema nervioso central y también se pueden expresar en plaquetas, placenta, endotelio pulmonar, mastocitos (51) y linfocitos (52,53).
Anteriormente, las plaquetas solían ser un modelo de las neuronas serotoninérgicas (54), debido a la detección y caracterización funcional de estos transportadores y de receptores 5TH2 en la membrana plasmática de este grupo celular. Además, se ha registrado un aumento o ausencia de modificaciones (55) de los receptores 5HT2 en las plaquetas de pacientes deprimidos con respecto a la de controles sanos (19).
Sin embargo, se ha confirmado que existen diferencias significativas entre los transportadores de 5HT de las plaquetas sanguíneas y los de las neuronas serotoninérgicas del sistema nervioso central (SNC). La regulación de la función de transportadores de 5HT en células no nucleares (como las plaquetas) no puede ser igual que en células nucleares (53).
Sustentado en lo anterior, y basándose en la presencia de inervación noradrenérgica del tejido linfoide (56) -lo cual sugeriría una importante conexión entre el sistema nervioso central y el sistema inmune-, se demostró la expresión de un transportador de 5HT de alta afinidad en linfocitos humanos de sangre periférica.
Al caracterizar el transportador de serotonina en Linfocitos T de sangre periférica de seres humanos, se evidenció que sus propiedades son similares al transportador de 5HT en el tejido neuronal (57). Este es un sistema de transporte activo y muestra dependencia al sodio (Na+) y a la temperatura. Cuando el Na+ es reemplazado por iones de colina, las tasas de recaptación de 5HT disminuyen en un 90%. La ouabaina, inhibidor de la bomba Na+/ K+ ATPasa, priva marcadamente la recaptación de 5HT. Por otra parte, se observa que la recaptación por linfocitos humanos muestra una dependencia del Cloro (CL-) (53), característica de los transportadores de neurotransmisores en el cerebro. (58).
La fluoxetina, fluvoxamina y clomipramina, inhibidores específicos de los transportadores de 5HT (59), poseen alta potencia inhibitoria de la recaptación de 5HT en linfocitos humanos (53).
 De
acuerdo con la sensibilidad a fármacos antidepresivos se han descrito
dos tipos de transportadores: uno localizado en la membrana plasmática
celular y otro en las vesículas citoplasmáticas de linfocitos
humanos de sangre periférica, siendo el transportador de la membrana
citoplasmática más sensible a dichos fármacos. (24).
De
acuerdo con la sensibilidad a fármacos antidepresivos se han descrito
dos tipos de transportadores: uno localizado en la membrana plasmática
celular y otro en las vesículas citoplasmáticas de linfocitos
humanos de sangre periférica, siendo el transportador de la membrana
citoplasmática más sensible a dichos fármacos. (24).
Este hallazgo plantea el uso de linfocitos para determinar la presencia de alteraciones neuroquímicas que pudieran conducir a la evaluación periférica de los trastornos psiquiátricos (37,52), facilitando las investigaciones relativas a esta área.
De esta forma, se ha descrito la importante relación entre el sistema inmune y la serotonina, evidenciándose así que el sistema nervioso central y el sistema inmunológico están íntimamente ligados. El área dedicada a estudiar este enlace es la psiconeuroimnunología, demostrando que una perturbación en un sistema puede ser reflejada en el otro (60).
Esta interacción ha sido documentada en distintos niveles, como por ejemplo, la modulación del eje hipotalámico-pituitario-suprarrenal por neurotransmisores o por citoquinas, y también por la expresión de marcadores neurales en una variedad de células del sistema inmune (52).
Esta interacción no sólo es bidireccional, a nivel central, y directa, mediante inervación autonómica; además, se ve afectada por la presencia de receptores de neurotransmisores en células del sistema inmune, ya que se ha demostrado la presencia de receptores 5HT1A y del correspondiente ARN mensajero en linfocitos humanos activados (47), así como la expresión de otros subtipos de receptores de 5HT.
Igualmente, se han descrito en linfocitos circulantes de la rata receptores como los B-adrenérgicos (61) y los colinérgicos muscarínicos, entre otros (62).
Un antagonista de los receptores 5HT1A, el pindobind, incrementa la producción de AMPc en células T humanas (47), lo que indica un efecto tónico de la 5HT sobre estos receptores en el linfocito. La 5HT periférica influye sobre la respuesta inmune a través de varios mecanismos. La inhibición de la síntesis de 5HT disminuye la proliferación celular estimulada por la IL-2 y el precursor de la síntesis de 5HT, el 5-Hidroxitriptófano, revierte el efecto (47). Por otra parte, se ha reportado la existencia de receptores 5HT1A en otros tipos celulares, y mediante estos receptores, la 5HT incrementa la citotoxicidad de las células natural killer sobre células blanco como los mononucleares (63). Además, los receptores 5HT2A estimulan la hipersensibilidad retardada de las células T efectoras (64) al tiempo que disminuyen la secreción de IL-16 de linfocitos T CD8+ (46).
En el trastorno depresivo mayor se ha demostrado la reducción en el número de transportadores de 5HT de linfocitos de sangre periférica de pacientes con depresión mayor (37), además de la disminución del transportador de 5HT en cerebro postmortem y en plaquetas de pacientes con esta enfermedad (19).
Asimismo, se han documentado alteraciones significativas en las funciones inmunológicas en la depresión mayor (65), entre las cuales se halla un incremento en el contaje de monocitos. En los pacientes con esta patología, la respuesta favorable a antidepresivos disminuye el número de monocitos sanguíneos (66).
Por otra parte, las citoquinas proinflamatorias, tales como la IL-1, la IL-6 y el IFN-gamma, se incrementan, situación que persiste incluso después del tratamiento (67). Se observa también un aumento de las células natural Killer (68). Cabe destacar que el tratamiento con amitriptilina en pacientes con depresión mayor, en los que se registran elevados niveles de IL-6 y del factor de necrosis tumoral-? en sangre total, reduce los niveles del último y sólo disminuye los de IL-6 en los pacientes que responden clínicamente al tratamiento (69).
En la depresión mayor existe un compromiso inmunológico con repercusiones bidireccionales, demostrado fehacientemente (70). Por esta razón, resultaría interesante estudiar los marcadores del sistema nervioso central presentes en las células circulantes del sistema inmune, debido a la poca información que se tiene sobre sistemas de neurotransmisores en linfocitos de sangre periférica y sus funciones.
No menos importantes son los factores psicosociales en la expresión de la enfermedad. En este sentido, se ha observado que los primeros episodios depresivos aparecen luego de algún acontecimiento estresante, y el estrés que acompaña al primer episodio produce cambios a largo plazo en la biología cerebral. Estos cambios de larga duración pueden producir variaciones en el funcionamiento de diferentes neurotransmisores y sistemas de señales intraneuronales, variaciones que implican pérdidas neuronales y disminución de conexiones sinápticas. Como consecuencia, la persona resulta más vulnerable para sufrir episodios depresivos posteriores, incluso sin factores estresantes externos (32).
Los acontecimientos vitales desempeñan un papel esencial o primario en la depresión. Estas situaciones comprenden la muerte de un familiar próximo o de un amigo, alguna enfermedad crónica en el mismo paciente o en un familiar, problemas interpersonales, dificultades financieras, divorcio, entre otras (9).
En resumen, la etiología de la depresión mayor demuestra la intervención de múltiples factores, como los genéticos, biológicos y psicosociales, lo que hace de esta enfermedad una patología compleja.
Por lo tanto, su tratamiento deberá basarse en la compresión de su etiología, integrando para ello la farmacoterapia y las intervenciones psicoterapéuticas. La farmacoterapia se basa en el uso de antidepresivos, entre los cuales encontramos principalmente a los inhibidores selectivos de la recaptación de serotonina, antidepresivos triciclitos (ATC) y a los inhibidores de la monoamino oxidasa (IMAO). En la actualidad, los más utilizados pertenecen al primer grupo, debido a su alta eficacia y a sus bajos efectos colaterales. Los ISRS incluyen fármacos como la fluoxetina, citalopram, sertralina y fluvoxamina (18)
![]()