

El proceso visual y su cascada de señalización
El proceso visual comienza con la conversión de paquetes de energía electromagnética llamados fotones o cuantos de luz, a una señal que puede ser analizada por el cerebro. Esta conversión es llevada a cabo por las células fotorreceptoras del ojo, un conjunto de células especializadas que se localizan en la retina.
En el ojo de la mayoría de los vertebrados existen dos tipos de células fotorreceptoras: los bastoncillos y los conos. Como se ilustra en la figura 1, los bastoncillos son células cilíndricas y tienen mayor tamaño, mientras que las células cónicas, más pequeñas, son los conos. Los bastoncillos median la visión en luz tenue formando imágenes en blanco y negro, y son tan sensibles que pierden la capacidad de transmitir señales en condiciones de luz diurna. Los conos, por su parte, operan eficientemente a niveles luminosos elevados y permiten la percepción del color.

Figura 1. Las células
fotorreceptoras del ojo. Los bastoncillos y los conos de la
retina de una salamandra se muestran aumentados en una
fotografía tomada mediante el uso de un microscopio
electrónico. Las células cilíndricas son los bastoncillos y
las células cónicas, más pequeñas, son los conos. Tomado de
Schnapf y Baylor (1987)
.
Los bastoncillos y los conos difieren tanto morfológicamente como en su función, pero mantienen ciertas semejanzas (Fig. 2). La parte superior de las células, el segmento externo, contiene los pigmentos que detectan y absorben la luz, así como toda la maquinaria molecular encargada de la transmisión de la señal y del inicio del impulso nervioso. La parte inferior, el segmento interno, contiene los organelos y el núcleo, y está especializado en la generación de la energía que requiere la célula para su funcionamiento, y en la renovación de las moléculas necesarias en el segmento externo. Además, el segmento interno incluye una terminación sináptica que provee la base para la comunicación con las otras células de la retina.
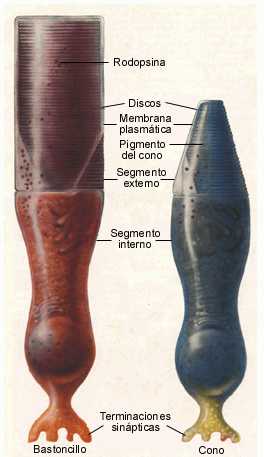
Figura 2. Los bastoncillos y
los conos difieren tanto en forma como en función pero mantienen
ciertas similitudes. La parte superior de las células, el
segmento externo, contiene los pigmentos que absorben la luz; la
parte inferior, el segmento interno, contiene los organelos y el
núcleo. La terminación sináptica conecta las células
fotorreceptoras a otras células de la retina. Tomado de Schnapf
y Baylor (1987).
Si una retina aislada es agitada ligeramente, los segmentos externos de las células fotorreceptoras se desprenden y la maquinaria de excitación visual puede ser estudiada en una forma altamente purificada. Debido a su mayor número, muchos estudios en el campo de la visión se han concentrado en los bastoncillos. Los segmentos externos de los bastoncillos son tubos angostos llenos de aproximadamente 2.000 discos apilados. Los estrechos discos contienen grandes cantidades de las proteínas que absorben la luz e inician la respuesta de excitación. La membrana externa, por otro lado, sirve para convertir la señal química en una señal eléctrica.
Embebido en la membrana lipídica de los discos de los segmentos externos de los bastoncillos se encuentra el pigmento visual denominado rodopsina, el cual representa el 80% del total de las proteínas celulares, y al menos el 95% de las proteínas de las membranas del segmento externo (Fig.3). La rodopsina contiene dos componentes, una porción proteica llamada opsina, y el cromóforo 11-cis-retinal, que es un derivado de la vitamina A. Ambos componentes se encuentran unidos covalentemente a través de una base de Schiff protonada entre el grupo e -amino de la Lys296 de la opsina y el grupo aldehído del retinal.
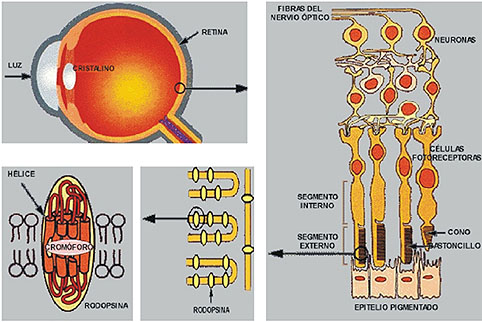
Figura 3. Esquema
representativo de la ubicación de la rodopsina en la membrana de
los segmentos externos de los bastoncillos de la retina. Tomado
de Schertler (1998).
La elucidación de la secuencia de aminoácidos de la rodopsina condujo a la propuesta de un modelo topográfico, que se basa en la presencia de siete regiones de aminoácidos predominantemente hidrofóbicos separados por regiones conectoras de residuos predominantemente hidrofílicos. La presencia de estas siete regiones sugirió que la rodopsina contiene siete hélices a que atraviesan la bicapa lipídica, e identificó a la rodopsina como uno de los miembros de la superfamilia de receptores tipo serpentina, que funcionan acoplados a proteínas enlazadoras de nucleótidos de guanina o proteínas G.
Las proteínas G son heterotrímeros compuestos de subunidades a , ß y g . Existen muchos productos génicos codificando para estas subunidades (hasta la fecha se han descubierto 20 a , 6 ß y 12 g ); sin embargo, sólo cuatro clases principales de proteínas G han sido definidas: GS, GI/Go, Gq, y G12/G13. Las proteínas G juegan un papel regulador importante en un gran número de mecanismos de transmisión de señales, acoplando proteínas receptoras transmembranales de siete hélices (GPCRs), a proteínas efectoras específicas. Miles de receptores GPCRs se conocen, y muchos más están siendo descubiertos todo el tiempo. Estos receptores serpentina están involucrados en el reconocimiento de señales tan diversas como la luz, el Ca2+, los olores, ciertas moléculas pequeñas que incluyen aminoácidos, nucleótidos y péptidos, y algunas proteínas; controlando así la actividad de enzimas, canales iónicos, y el transporte de vesículas, vía catálisis del intercambio de GDP por GTP sobre sus correspondientes proteínas G. Dentro del plan arquitectónico común de los GPCRs, los lazos intracelulares que conectan las hélices a transmembranales, constituyen el dominio de enlazamiento de las proteínas G. Aunque aún no ha sido determinada la estructura de alta resolución de ningún receptor acoplado a proteína G, las estructuras de difracción electrónica de baja resolución de las rodopsinas de bovino y de rana, publicadas en la década pasada, muestran la posición y orientación de estas siete hélices a en la rodopsina (Fig. 4). Experimentos bioquímicos y de mutagénesis, con una variedad de GPCRs, sugieren que la activación del receptor causa cambios en las orientaciones relativas de las hélices transmembranales 3 y 6, como producto del enlazamiento de su ligando. Estos cambios afectan la conformación de los lazos intracelulares que interactúan con las correspondientes proteínas G, poniendo al descubierto los sitios de enlazamiento de dichas proteínas, previamente enmascarados.
Figura 4. Densidades de
proyección en dos dimensiones de la estructura de la rodopsina. Abajo
se muestra esquemáticamente el arreglo tentativo de las siete
hélices a transmembranales de la proteína. Tomado de Schertler
(1998).
Volviendo al proceso de excitación visual, el primer evento en este mecanismo es la absorción de un fotón por el cromóforo 11-cis-retinal de la rodopsina, lo que produce su isomerización a la forma todo-trans. Este evento ocurre mediante una serie de transformaciones fotoquímicas de la rodopsina que conllevan a la aparición de diversos fotointermediarios, los cuales poseen absorción óptica máxima característica. Finalmente, el último fotointermediario es hidrolizado a opsina y todo-trans retinal. La cascada visual está mediada por la metarodopsina II que es el fotointermediario responsable de transmitir la señal luminosa a las otras proteínas de la ruta de señalización visual, y es por ello que es considerada la rodopsina fotoexcitada o fotoactivada (R*).
El siguiente paso en la excitación visual es la activación de la transducina por R*. La transducina es una proteína periférica de la membrana que pertenece a la familia de las proteínas G heterotriméricas, y como tal posee tres cadenas polipeptídicas conocidas como las subunidades a (Ta ), b (Tb ), y g (Tg ). Por sus características estructurales ha sido clasificada como una proteína G tipo GI/Go. A oscuras, la transducina se encuentra en su forma inactiva, enlazada a GDP. Por efectos de la luz, R* interacciona fuertemente con la transducina ligada a GDP. R* promueve el intercambio de GDP por GTP sobre la unidad Ta , formándose primero un intermediario en el cual R* está unido a la transducina con su bolsillo de enlazamiento de nucleótidos vacío, y luego un complejo de la R* con la transducina ligada a GTP. Ta -GTP constituye la forma activada de la transducina (Ta *). Ta *-GTP disminuye su afinidad tanto por Tb g , como por R*, y estos cambios en afinidades son críticos para el proceso de excitación. La liberación de la rodopsina fotoestimulada de su complejo con la transducina permite que R* actúe catalíticamente e interaccione con otras transducinas, activándolas. Cerca de 500 moléculas de Ta *-GTP pueden ser formadas por acción de una simple molécula de R*. La activación de la transducina es la primera etapa de amplificación en este proceso (Fig. 5).
Figura 5. Resumen diagramático
de la cascada enzimática de excitación visual.
Se muestran los principales ciclos bioquímicos involucrados en
el proceso de fototransducción. R = rodopsina, T = transducina,
PDE = fosfodiesterasa de GMP cíclico, I = subunidades
inhibitorias de la PDE, R*-kinase = rodopsina quinasa,
A = arrestina, y P = fosfato inorgánico. Los asteriscos ilustran
los estados activados de las proteínas. Tomado de Hargrave
(1993).
La disociación de la transducina en sus subunidades permite a Ta *-GTP transportar la señal de excitación a la siguiente enzima en la cascada, la fosfodiesterasa de GMP cíclico (PDE). Ta *-GTP activa a la PDE, al liberarla de la inhibición impuesta por sus subunidades g o I reguladoras (Fig. 5). La PDE activada (PDE*) cataliza la hidrólisis de GMP cíclico (cGMP) a 5’-GMP. Miles de moléculas de cGMP pueden ser hidrolizadas rápidamente a partir de una molécula de PDE*, y en consecuencia, este evento se considera el segundo paso de amplificación de la cascada visual.
¿Cuál es el efecto de la hidrólisis de cGMP por la PDE*?. En la oscuridad, la concentración total de cGMP es alta. Bajo estas condiciones, el cGMP mantiene abiertos los canales catiónicos presentes en la membrana plasmática de los bastoncillos, permitiendo la "corriente oscura" producto del transporte de iones de Na+ y Ca2+ que despolarizan la célula. La hidrólisis de cGMP por efecto de la fotoactivación de la PDE causa el cierre de los canales, reduciendo así la corriente circulante. Es por ello que la membrana plasmática sufre una hiperpolarización en respuesta a una señal luminosa. Estos cambios de voltaje son comunicados a las células contiguas, localizadas en la retina, por transmisión química a través de las terminaciones sinápticas de las células fotorreceptoras.
Hay varios eventos que regulan esta cascada. Por un lado, la actividad GTPasa inherente a Ta convierte a Ta *-GTP en Ta *-GDP, lo que produce la desactivación de la PDE*, y promueve la reconstitución de la forma holoenzimática de la transducina para que el ciclo se repita. Proteínas tales como la RGS 9 (o proteína reguladora 9 de la señalización de las proteínas G), así como la subunidad inhibitoria g o I de la PDE, actúan como proteínas GAPs que funcionan estimulando dicha actividad GTPasa. Sin embargo, el ciclo regenerador de la transducina puede ser interrumpido por la acción de una fosfoproteína llamada fosducina. La fosducina, en su estado desfosforilado, es capaz de enlazarse selectivamente a Tb g y formar un complejo muy estable. Al bloquear el enlazamiento de Ta a Tb g , y evitar la reconstitución de la transducina heterotrimérica, la fosducina permite que Ta *-GTP actúe por mayor tiempo, y no sea reciclada tan rápidamente. Este evento está controlado por procesos de fosforilación y desfosforilación mediados por la proteína quinasa dependiente de AMP cíclico y una proteína fosfatasa aún no determinada. La hidrólisis del GTP enlazado a Ta es necesaria pero no suficiente para restituir el sistema a su estado de oscuridad. El decaimiento espontáneo de R*, correlacionado con la liberación del cromóforo, es muy lento. Como también se muestra en la figura 5, existe un proceso más rápido de inactivación, el cual es dependiente de ATP. Este proceso se basa en la fosforilación de R* por una proteína quinasa específica, la rodopsina quinasa (R*-Kinase), seguida por el enlazamiento de una proteína soluble, la arrestina (A), la cual reconoce a la R* fosforilada en una serie de residuos de Ser y Thr presentes en su extremo COOH-terminal. La arrestina detiene la acción de R* al bloquear competitivamente el enlazamiento de la transducina a la rodopsina fotoactivada. El estado oscuro de la rodopsina ligada a 11-cis-retinal es regenerado por una serie de reacciones que involucran la hidrólisis de la unión tipo base de Schiff, la disociación del todo-trans retinal, la disociación de la arrestina, la desfosforilación de la rodopsina fosforilada por una proteína fosfatasa tipo 2A específica de los bastoncillos, y finalmente el re-enlazamiento del 11-cis-retinal.
El Ca2+ también ejerce efectos muy importantes en la cascada de señalización visual. Los niveles citosólicos de calcio disminuyen en presencia de luz, no solamente porque cesa su entrada a través de los canales sensibles a cGMP, sino también porque su eflujo se mantiene constante a través de una proteína intercambiadora de Na+/Ca2+ localizada en la membrana plasmática de los bastoncillos. Cuando la concentración de calcio disminuye por debajo de 10 nM, se estimula una proteína guanililo ciclasa, localizada también en la membrana, la cual sintetiza cGMP a partir de GTP. Esto conlleva a la recuperación de los niveles de cGMP presentes en el estado de oscuridad. Además, existen otras proteínas moduladoras de la cascada de excitación, las cuales funcionan de una manera dependiente de la concentración de calcio. Por un lado la calmodulina regula directamente los canales catiónicos de compuerta dependientes de cGMP. Otra proteína llamada recoverina, regula la acción de la rodopsina quinasa de una manera dosis-dependiente de calcio. Finalmente, también existen varias proteínas activadoras de la guanilio ciclasa, llamadas proteínas GCAP’s, las cuales modulan la acción de esta enzima de una forma dependiente de la concentración del ion divalente.
